Les conditions de mise sur le marché
L’autorisation de mise sur le marché (AMM) des biosimilaires, comme pour tout produit biologique est centralisée par l’Agence Européenne du Médicament (EMA).
Cette AMM est accordée sur la base d’une équivalence au médicament biologique de référence en termes de résultats pharmacologiques et cliniques, de qualité et de sécurité.
Le demandeur d’une AMM doit démontrer qu’il n’existe aucune différence significative avec le médicament de référence en réalisant des essais précliniques et cliniques supplémentaires par rapport à ceux nécessaires à l’obtention d’une AMM d’un médicament de référence.
Les bénéfices
Les coûts de production d’un médicament biosimilaire sont moins élevés que pour un médicament de référence.
Le médicament biosimilaire permet de diversifier l’offre de médicaments biologiques pour une pathologie donnée et de limiter les risques de rupture de stock.
Le marché devient moins sensible aux accidents de production.
Ainsi, ils permettent un accès à l’innovation pour un plus grand nombre de patients.
Les économies réalisées permettent de libérer des fonds pour d’autres médicaments innovants et couteux.
La différence entre médicaments chimiques et biologiques
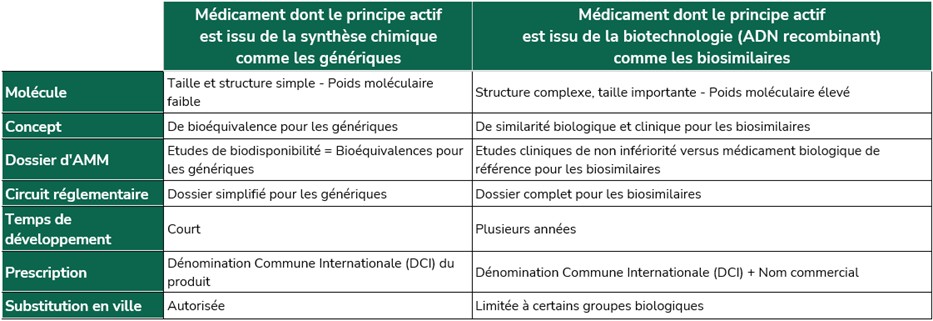
La prescription
La prescription est possible par le médecin autorisé, dans le respect des indications de l’AMM du médicament.
Les doses et le schéma d’administration sont identiques à ceux du médicament de référence.
L’interchangeabilité
Le prescripteur peut remplacer un médicament biologique par un autre figurant sur la liste des médicaments biosimilaires de l’ANSM, cet acte médical est appelé « interchangeabilité ».
Ce changement peut avoir lieu à tout moment du traitement. Il doit être raisonné et tenir compte de l’état du patient.
Dans le cadre de l’interchangeabilité, les règles habituelles de bonne prescription doivent être respectées :
- informer le patient,
- veiller à une surveillance clinique appropriée lors du traitement,
- assurer une traçabilité des médicaments prescrites dans le dossier médical du patient.
La substitution
Le projet de loi de financement de la sécurité sociale pour 2022 a introduit la possibilité de substituer des médicaments biologiques (médicament de référence et médicament biosimilaire) par le pharmacien selon certaines conditions :
1- Le médicament biologique similaire délivré appartient au même groupe biologique similaire que le médicament biologique prescrit ;
2- Ce groupe biologique similaire figure sur une liste accompagnée le cas échéant de conditions de substitution et d’information du prescripteur et du patient, fixée par un arrêté conjoint des ministres chargés de la santé et de la sécurité sociale pris après avis de l’ANSM ;
3- Le prescripteur n’a pas exclu la possibilité de cette substitution par une mention expresse et justifiée portée sur l’ordonnance, tenant à la situation médicale du patient ;
4- Lorsque le pharmacien délivre par substitution au médicament biologique prescrit un médicament biologique similaire du même groupe, il inscrit le nom du médicament qu’il a délivré sur l’ordonnance et informe le prescripteur et le patient de cette substitution.
5- Le pharmacien assure la continuité de la dispensation du même médicament lors des dispensations suivantes
La procédure :
- Le pharmacien inscrit le nom du médicament qu’il a délivré sur l’ordonnance ;
- Le pharmacien procède à l’enregistrement du nom du médicament dispensé par substitution et de son numéro de lot et informe le prescripteur et le patient de cette substitution.
Cette substitution ne doit pas entraîner une dépense supplémentaire pour l’assurance maladie supérieure à la dépense qu’aurait occasionnée la délivrance du médicament biologique similaire le plus onéreux du même groupe.
L’ANSM a émis plusieurs avis sur les conditions de mise en œuvre de la substitution au sein des groupes biologiques similaires:
- Le 10/09/2024: groupes biologiques similaires ranibizumab et aflibercept.
- Le 26/11/2024: groupes biologiques similaires tériparatide, étanercept et adalimumab.
- Le 20/12/2024: groupes biologiques similaires follitropine alfa, époétine, énoxaparine et insuline.
La substitution ne devient possible qu’après publication d’un arrêté du ministre chargé de la Santé.
À noter que l’ANSM a exclu la substitution au sein des groupes biologiques similaires insuline asparte, insuline glargine et insuline lispro.
Les groupes similaires pour lesquels la substitution est désormais possible sont :
- filgrastim
- pegfilgrastim
- ranibizumab
- tériparatide
- etanercept
- adalimumab
- énoxaparine
- follitropine alfa
- époétine
- aflibercept
- ustékinumab
L’arrêté d’inscription de chaque groupe similaire peut comporter des restrictions concernant les indications concernées par la substitution.
Par exemple, pour l’ustékinumab, la substitution n’est possible que dans le périmètre de l’AMM de la spécialité délivrée.
Il convient de respecter les arrêtés publiés au Journal Officiel.
La liste des spécialités commercialisées (dernière mise à jour 2 mars 2026) et un mémo d’aide à la pratique sont disponibles sur le Site ameli.fr



